핵산 합성은 고체상 시알산 아미드 트리글리세리드 방법을 사용하여 수행됩니다. DNA의 3' 말단을 고체상 기판에 고정하고 원하는 DNA 단편이 합성될 때까지 뉴클레오티드를 3'에서 5' 방향으로 추가합니다. .이는 DNA 중합효소를 적용하여 DNA를 합성하는 것과 다릅니다.
첫 번째 염기의 3' 말단은 합성 중에 CPG에 고정되고, 다음 염기의 5'-OH는 di-p-tolyl trityl DMT로 보호되고, 염기의 아미노기는 벤조산으로 보호되고, 3'은 -OH는 아미노 인산염 화합물로 활성화됩니다.5의 1개 염기의 1개 염기의 5'-OH와 다음 염기의 3'-OH가 포스파이트 트리글리세리드를 형성하고, 이것이 요오드에 의해 산화되어 인산 트리글리세리드로 바뀌고, 두 번째 염기의 5'-OH에 있는 보호제는 다음과 같이 제거됩니다. 디클로로아세트산 첨가 다음 염기 첨가를 통해 DM 사이클, 합성 후 약산으로 5'-OH에 있는 보호제가 제거됨 농축된 수산화암모늄으로 조각이 고체 수지에서 분리되고 염기에서 보호제가 제거됨 진한 수산화암모늄으로 가열하여 수산화암모늄을 제거하고, 단편을 진공건조한 후, 액체 크로마토그래피 또는 PAGE로 핵산을 정제한다.
올리고 합성 단계
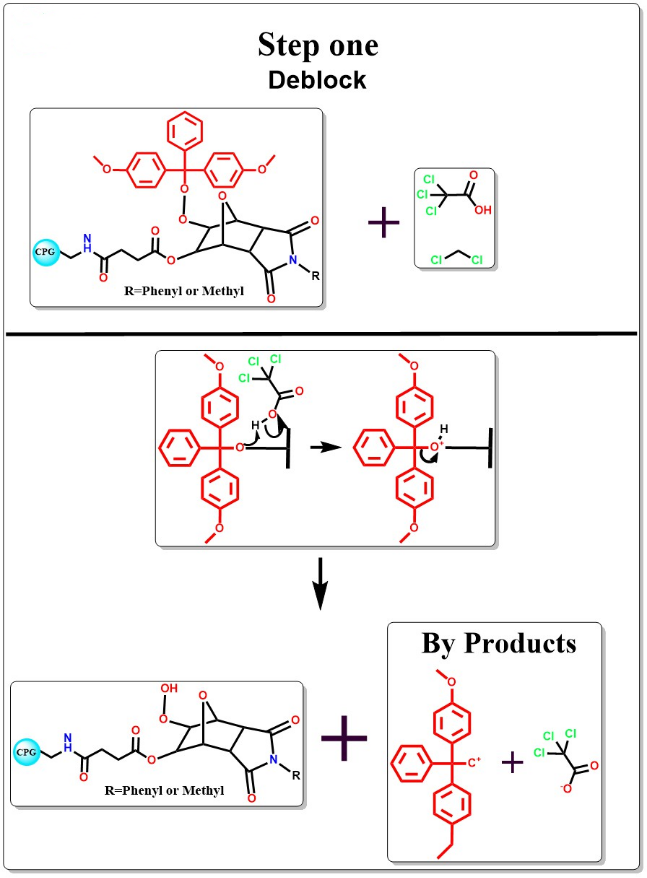
디블로킹
그만큼TCA 용액을 첨가하면 5말단 DMT 보호기가 제거됩니다.
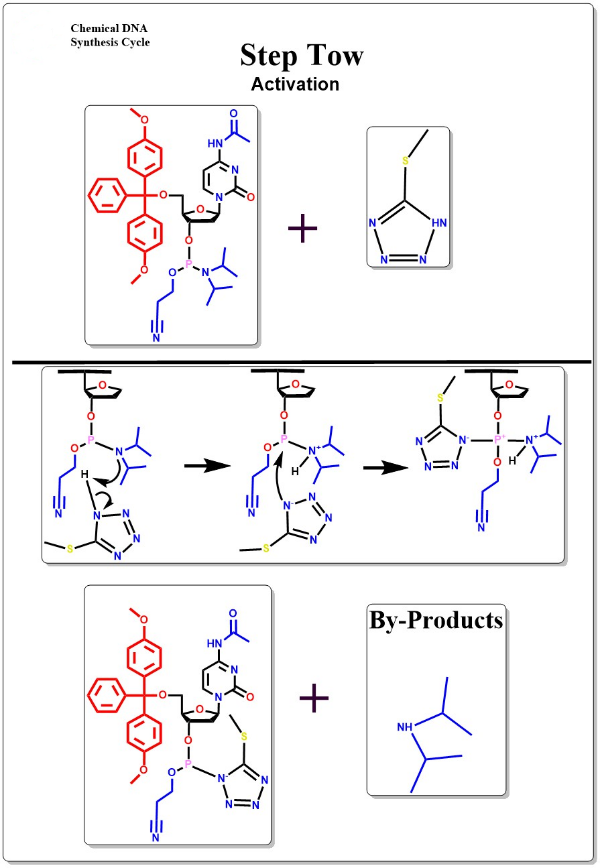
활성화
활성 올리고뉴클레오티드 단량체 중간체를 형성하기 위해 활성화제를 올리고뉴클레오티드 단량체와 혼합하는 단계.
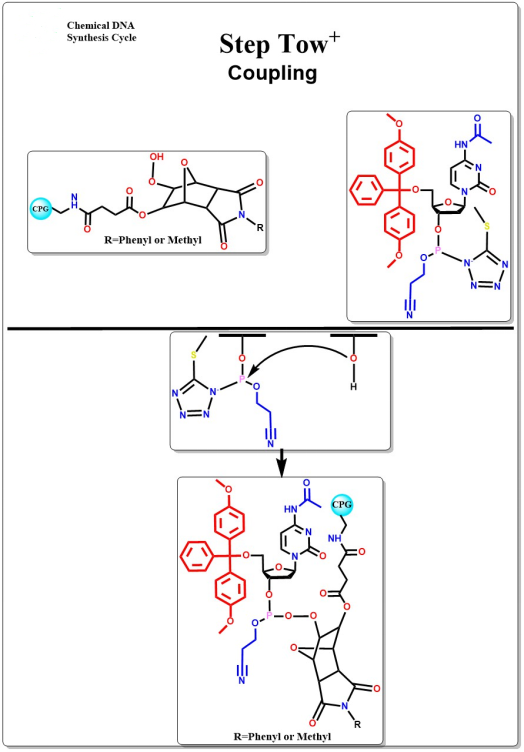
커플 링
5-말단 수산기는 항생성 축합 반응에서 활성 올리고뉴클레오티드 중간체와 반응하여 불안정한 포스파이트 트리글리세리드 결합을 형성합니다.
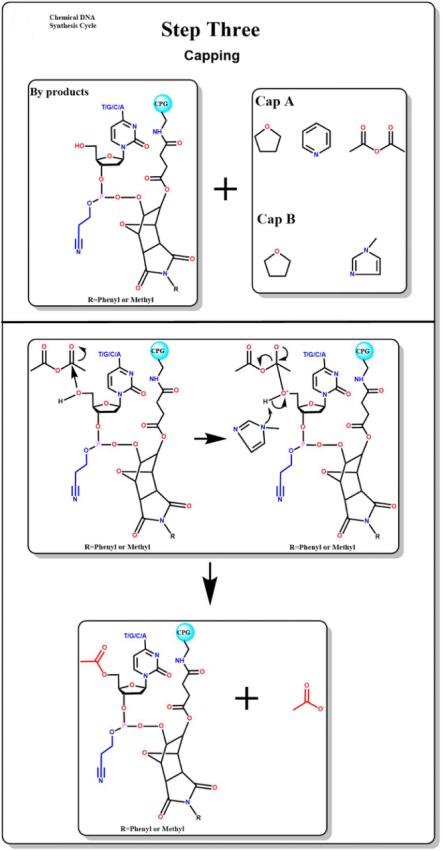
캡핑
캡핑제를 첨가하면 축합 반응에 관여하지 않는 과잉 수산기와 아세틸화 캡핑 반응이 수행됩니다.
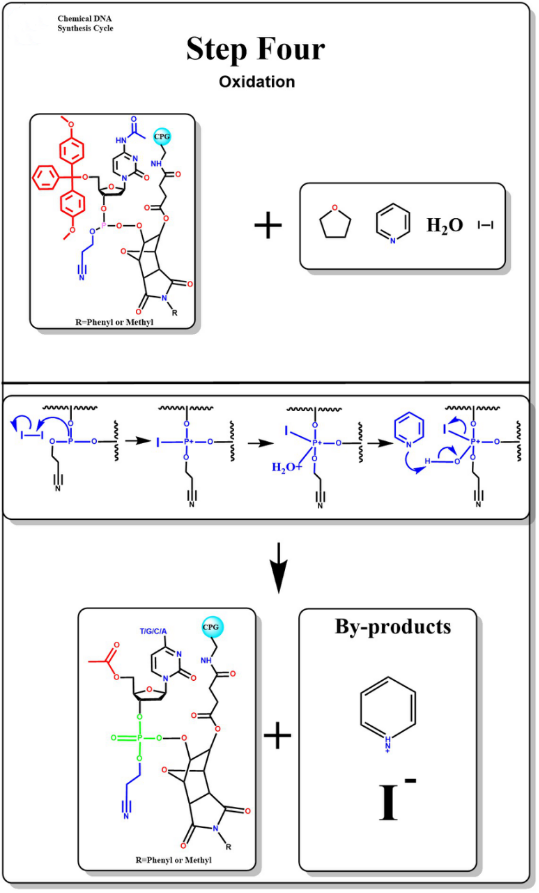
산화
물을 함유한 요오드 용액을 첨가하면 산화에 의해 불안정한 인산염 결합과 반응하여 안정한 인산 트리글리세리드 결합이 형성됩니다.
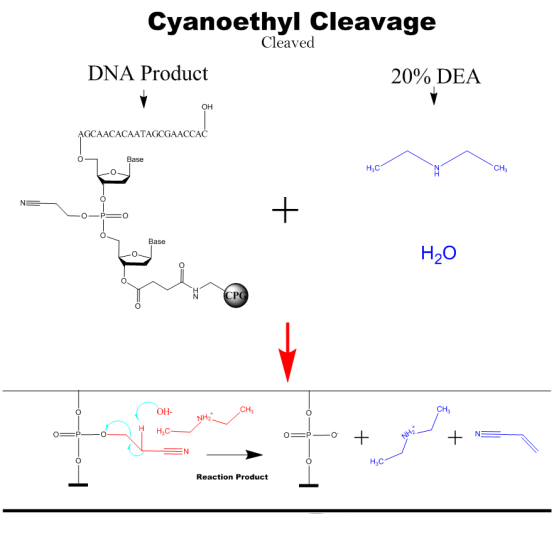
시아노에틸 절단
합성 후 핵산 생성물에 DEA 용액을 첨가하여 인산염 트리글리세리드 결합에서 시아노에틸 그룹을 제거합니다.
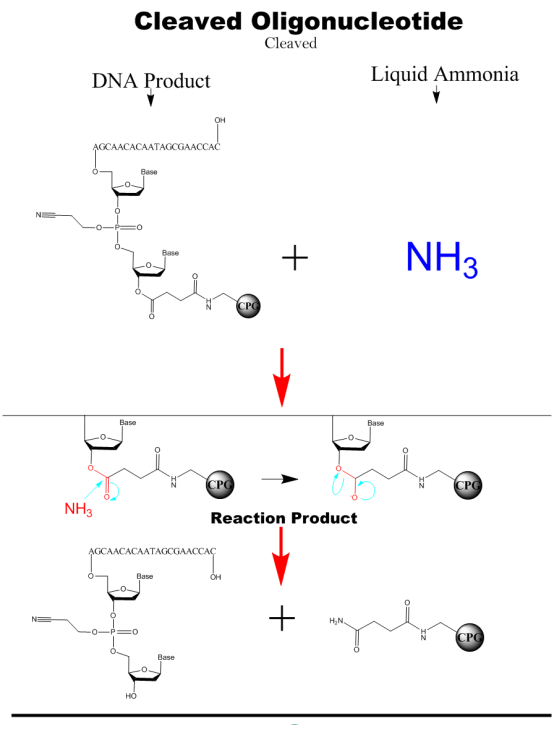
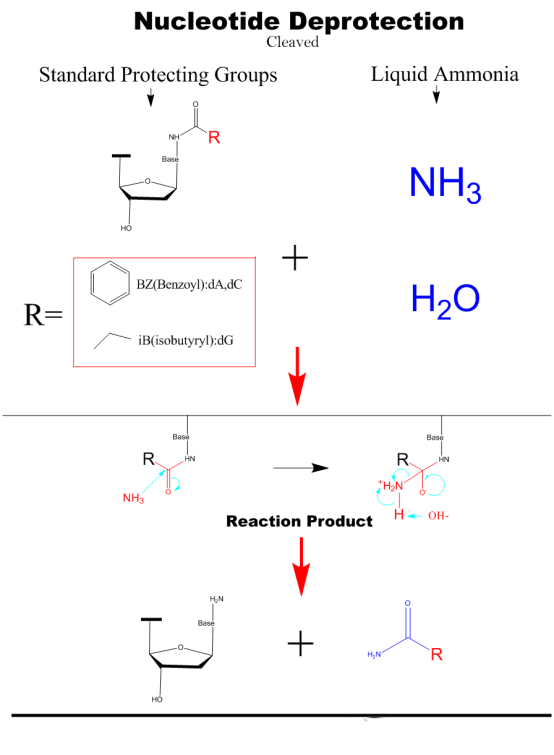
절단 및 보호 해제
농축된 수산화암모늄 용액을 첨가하여 핵산 단편을 고체상 담체에서 분리한 다음 가열하여 염기의 수소 결합에서 보호기를 제거합니다.
게시 시간: 2022년 11월 21일